理科【化学】
物質の性質(気体・水溶液・状態変化)
-
おもな気体の集め方のなかで、水素の集め方は「水上置換法」と書かれていることがあるのですが、水素は空気より軽いので「上方置換法」で集めてはいけないのですか?
-
水素は、空気よりずっと軽いという特徴がありますが、ほかに水に溶けにくいという特徴もあります。ですので、集め方は「上方置換法」でも「水上置換法」でもどちらでもいいように感じますね。
ですが、原則として、水に溶けにくい気体であれば、空気より重いものも軽いものも「水上置換法」で集めます。なぜなら、下方置換法や上方置換法に対して、水上置換法は、集めるときに空気が混ざらないため、より純粋な気体を集めることができるからです。また、どれだけの体積を集めることができたかも判断しやすいですね。
気体とその集め方については、
・水に溶けにくい気体はすべて水上置換法
・水に溶けやすく、空気より重い気体は下方置換法
・水に溶けやすく、空気より軽い気体は上方置換法
と覚えておきましょう。
-
再結晶と蒸留の違いは何ですか?
-
再結晶と蒸留では,最終的に取り出すものが違います。再結晶は固体,蒸留は液体を取り出します。
再結晶とは,溶解度の差を利用して,温度を下げたり水を蒸発させたりして,水溶液に溶けている「結晶」を取り出す方法のことです。
蒸留とは,混合物を物質の沸点の差を利用して分離する方法です。液体を沸騰させて,出てくる気体を冷やして,再び「液体」に戻して取り出します。
化学変化・原子と分子・酸化と還元
-
二酸化炭素はなぜ有機物に含まれないか。
-
有機物とは,基本的には炭素をふくむ化合物のことなのですが,例外があります。
もともとは,生物によってつくられ,燃やすと二酸化炭素を発生したり,炭ができたりするような物質を,生命に由来する,というような意味で「有機物」と呼び,それ以外の物質を無機物と呼んで区別していました。ここから成分の化学的な研究が進み,「炭素を含む」「炭素を含まない」によって,有機物と無機物を区別するようになりました。ですから,まず「炭素をふくむ化合物」というのが,有機物の最低条件ではあります。
ただ,炭素を含んでいてもすべてが有機物であるとは言えず,さらに「燃やすと二酸化炭素を発生する」「燃やすと炭ができる(酸素がなくなって炭素が残る)」などの特徴もあります。単純な見分け方はありません。基本的には,教科書や授業で出てきた物質について,有機物か無機物かを分類して覚えておきましょう。
以下が分類の例です。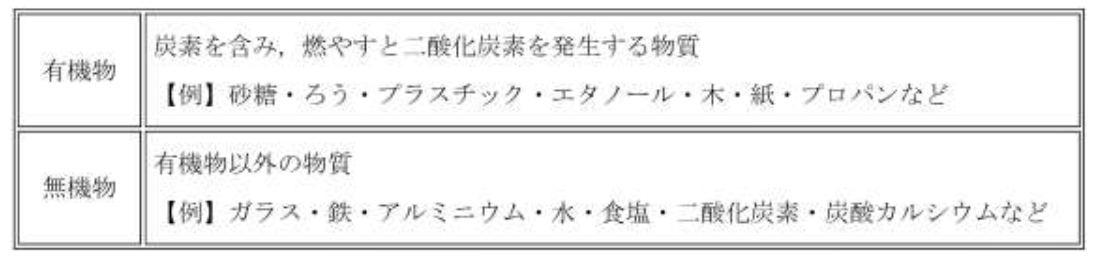
二酸化炭素以外にも,一酸化炭素,炭酸カルシウムなどは例外です。構造が簡単で有機物が示すような性質(燃えて二酸化炭素を発生するなど)をもっていないので,無機物に分類されています。
また,炭素は化合物ではなく単体なので,これも有機物には含めません。
-
「単体」「化合物」「混合物」「純粋な物質」の違いがよくわかりません。
-
単体とは、ただ1種類の原子でできている物質のことをいい、化合物とは、2種類以上の原子でできている物質のことをいいます。
一方、混合物とは、異なる2種類以上の物質が混じりあった物質です。逆に、1種類の物質だけで構成されているものを純粋な物質(単一の物質)といいます。
下に例としてあげた物質も含めて、単体と化合物は全て純粋な物質に含まれます。混合物の代表的な例としては、食塩水や空気などがあります。
食塩水は、食塩である塩化ナトリウム(化合物)と水(化合物)の交じり合った混合物、空気は、酸素(単体)や二酸化炭素(化合物)、窒素(単体)などの気体が交じり合った混合物ですね。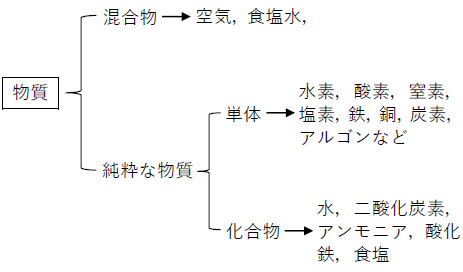
混合物・化合物の区別は、もとになる物質に分ける方法を考えると、その違いがわかりやすくなると思います。
混合物は、純粋な物質が混じり合っているだけなので、ろ過、再結晶、蒸留などの方法で分離することができますが、化合物は、2種類以上の原子が化学変化によって結びついたものなので、分解などの化学変化を起こさなければ、もとの物質を取り出すことはできません。
なお、分解とは、化学変化の一種で、化合の逆の現象です。混合物を2種類以上の物質に分けるのは、化学変化ではないので、注意しましょう。
-
分子をつくる物質とつくらない物質の違いを教えてください。
-
「分子をつくる物質」というのは、「ある限られた数の原子どうしがグループをつくり、それがその物質の最小単位となって存在する物質」のことです。
一方、「分子をつくらない物質」というのは、「原子がグループをつくらず、連続的に結合した状態で存在する物質」のことです。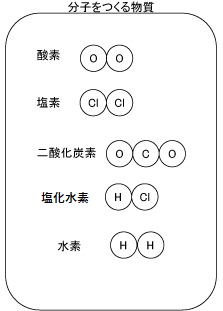
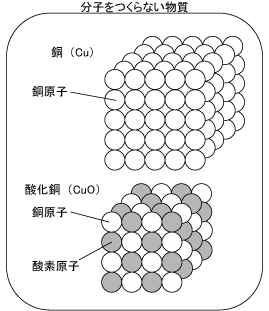
基本的に、非金属の物質は分子をつくることが多く、金属や金属の化合物は分子をつくりません。したがって、たとえば、金、銀、銅などは金属(単体でもある)ですので、分子をつくりません。これからの化合物も分子をつくりません。ただ連続的に原子が無数につらなった状態で存在します。つまり、すべての物質が分子の状態で存在しているわけではなく、単体にも化合物にも、「分子をつくる物質」と「分子をつくらない物質」とがあり、例外はありますが、すべての物質は与えられた環境の中で、一番安定した状態で存在しようとします。したがって、なぜ、酸素や二酸化炭素、水素などが分子をつくって存在するのか、と言えば、それらの物質にとっては、分子の状態で存在するのが一番、化学的に安定した状態でいられるからなのです。簡単に言ってしまえば、その物質にとって一番居心地のよい状態であるから、ということですね。
一方、銅や酸化銅、鉄や酸化鉄などのような、金属や金属の化合物は分子をつくらず、ただ、原子が連続的につながって存在しているものがほとんどで、これは、金属や金属の化合物にとっては、分子を作らず、原子が連続的につながって存在していた方が化学的に安定した状態であるからです。というわけで、これらの物質は、通常、分子にはならない、ということです。
-
フェノールフタレイン溶液について教えてください。
-
フェノールフタレイン溶液は、水溶液の性質を調べる薬品の物質名です。アルカリ性の水溶液と反応して色が変化するので、ある水溶液がアルカリ性かどうかを調べるために使われます。アルカリ性の強さが強いほど、濃い赤色に変化します。
「フェノールフタレイン」という名前は、この物質が「フェノール」と「無水フタル酸」という物質からできていることに由来しています。フェノールや無水フタル酸については、高校の化学でくわしく学習する機会がありますよ。
-
塩化コバルト紙に水をつけたときの反応は、青色→赤色ですか? それとも青色→桃色が正しいですか?
-
青色の塩化コバルト紙は水を吸収すると、色が変化します。
この変化後の色については教科書によって、赤色、うすい赤色、桃色、ピンク色など、いろいろな表記があります。これはどれも同じことを表しているので、どれも正しいです。
学校のテストや入試では、先生のご指導に従って、授業や教科書で習った通りに答えるといいでしょう。
-
化学式の順番は決まっているのですか?
-
中学ではくわしく学習しませんが、化合物の化学式では以下のようなルールにしたがって、元素の順番を決めています。
1.金属(亜鉛、マグネシウム、銅、ナトリウム、カルシウムなど)と非金属(塩素、酸素、水素、硫黄など)の化合物では、金属を先に書く。
たとえば酸化銀はAg2(銀は金属、酸素は非金属)、塩化ナトリウムはNaCl(ナトリウムは金属、塩素は非金属)、酸化マグネシウムはMgO(マグネシウムは金属、酸素は非金属)となります。2.非金属と非金属では、次の系列で、前にある元素記号を先に書く。
C, P, N, H, S, I, Br, Cl, O この法則にしたがうと、たとえば水はH2、アンモニアはNH3、二酸化炭素はCO2となります。3.原子団(NO3, OH, CO3, SO4)はあとに書くが、NH4だけは先に書く。
※原子団というのは、2種類の原子同士の結びつきが強くて、1つの原子のようになっているものです。
硫酸はH2SO4、水酸化ナトリウムはNaOH、塩化アンモニウムはNH4Clとなります。化合物の名称から化学式を考えるときは、物質名を後ろから前に化学式に置き換えてつくるというのが原則になります。
たとえば酸化銅は銅を表す「Cu」を先に書き、酸化を表す「O」をそのあとに続けて書いて、「CuO」と表します。
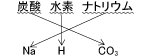
同様に炭酸水素ナトリウムは、ナトリウムを表す「Na」を書き、次に水素を表す「H」、炭酸を表す「CO3」をそのあとに続けて書いて、「NaHCO3」と表します。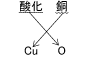
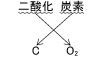
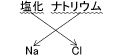
このような規則性はありますが、化合物の化学式は、ある程度は暗記してしまったほうがいいでしょう。いくつかを暗記して、頭に入ると、上で説明した規則性も理解しやすくなります。
-
化学反応式の書き方、ルールについて教えてください。
-
まず化学反応式で覚えておかなくてはならないことは、反応の前後で原子の種類と数を同じにしなければならないということです。
化学反応では、原子が何もないところから現れたり、逆に消滅したりすることはありません。あくまで原子はそのまま存在しつづけ、組合せ(結合)する相手が変わることによって、違う物質ができるのです。
化学反応式を正しく書くためには、何と何の物質を反応させると何と何ができるかについて覚え、それぞれの物質の化学式を書いて、原子の数を反応の前後で合わせる、という順序で進めます。まずは以下の化学式をしっかりと覚えましょう。
【覚えた方がよい化学式】
酸素 O2・水素 H2・水 H2O・塩素 Cl2・窒素 N2・二酸化炭素 CO2・アンモニア NH3・酸化銅 CuO・酸化マグネシウム MgO・酸化銀 Ag2O・硫黄鉄 FeS・塩化ナトリウム NaCl・塩酸 HCl・水酸化ナトリウム NaOH
他にも学校の教科書などに出てくる化学式は覚えておくようにしましょう。
ではこれら物質の化学式から、化学反応式を組み立てる方法を簡単な例(水素と酸素の化合)で示します。
1.化学変化の前後の物質名を書き出す。
水素 + 酸素 → 水(覚える必要あり)
2.化学式で表す。
H2 + O2 → H2O
これを原子のモデルで表してみると、以下のようになります。
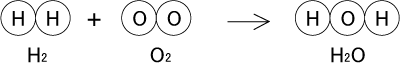
ここで、化学反応式では「左辺と右辺で、原子の種類と数が同じ」でなければいけなかったですね。この場合は、左辺と右辺で、水素原子の個数と酸素原子の個数が同じでなければいけないということです。
そこで係数(分子の数)を調節して、左辺と右辺で、水素原子と酸素原子の個数が同じになるようにするわけです。化学式は決まっているので変えてはいけません(小さい数字は変えてはいけません)。3.反応の前後で、原子の数が同じになるようにする。
左辺の酸素原子を合わせて、右辺の酸素原子を増やすには、水の化学式の係数を2にします。
①酸素の係数を合わせる。
H2 + O2 → 2H2O
すると、以下のようになります。
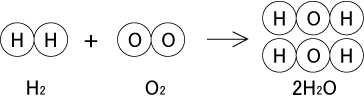
…でも、今度は右辺の水素原子が4個になってしまいました。
というわけで、今度は左辺の水素の化学式の係数を2にします。②水素の係数を合わせる。
2H2 + O2 → 2H2O
するとモデル図は次のようになり、やっと左辺と右辺の各原子の数がすべて等しくなりました。
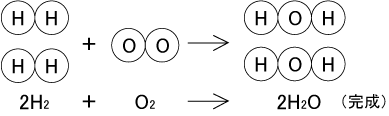
これが正しい化学反応式というわけです。
もう一つ例として「銀の酸化」について考えてみましょう。
銀は金属なので「Ag」と元素記号そのままでいいですが、酸素は「O2」と、2個結びついた分子になって存在すると決まっています。そして酸化銀は「Ag2」、つまり銀原子と酸素原子が2:1の個数の割合でできていると決まっています。
すると化学反応式はそのまま並べると、Ag + O2 → Ag2
となるわけですが、酸素原子が左辺で2個、右辺で1個になってはいけません。(反応の前後で原子の種類と数を同じにしなければいけないため)。かといって、酸化銀の化学式を「Ag2O2」にすることはできません(分子をつくる化学式は変えてはいけないため)。
そのため、酸化銀の分子全体を2個用意します。Ag + O2 → 2Ag2O
すると酸素原子は2個と2個でそろいましたが、銀原子は右辺で4個になりますので、左辺の銀原子も4個にしなくてはならないのです。
結果として、4Ag + O2 → 2Ag2O
となるわけです。
-
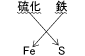
硫黄と鉄を混ぜ合わせた粉末を入れた試験管を加熱するとき、なぜ「粉末の上部」を加熱するのですか?
-
「鉄と硫黄の化合」の実験では、反応開始のきっかけとして、試験管上部を加熱します。いったん鉄と硫黄の反応が起こり始めると、それによって熱が出るので、外部から熱しなくても、反応は進んでいきます。このような反応を発熱反応といいます。
このとき下部を加熱すると、ガスバーナーの炎は、全体(あるいは混合物の多くの部分)を加熱することになります。その場合、反応が速く進みすぎてしまい、大量の熱が一度に発生するため危険です。つまり、反応の速さを制限するために、試験管の上部を加熱し、反応が始まったら加熱をやめるのです。
鉄と硫黄の反応の場合には、火山の噴火と同じくらいの温度(800℃以上)にもなるそうです。そのような熱が一度に発生したら、試験管も溶けてしまいますし、本当に危険ですね。また、発生する熱によって硫黄の一部が酸化し、有毒な二酸化硫黄が発生する可能性があります。試験管に脱脂綿でかるく栓をするのは、二酸化硫黄が出てくる恐れがないようにするためです。
この実験に限らず、理科の実験では危険をともなうことが多いので、注意事項を必ず守るようにしましょう。
イオン・電気分解・電池
-
電気分解で、どちらが陽極/陰極になるのかわかりません。
-
下の図で考えてみましょう。
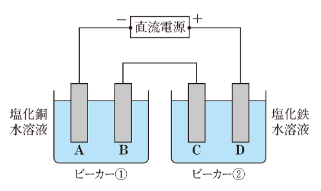
まず、電流が流れる向きと、電子が流れる向きについて復習しておきますと、電流は電源の+極から出て-極に入りますが、電子は-極から出て+極に入ります。
このことをふまえて、電子の流れる向きを図に示しました。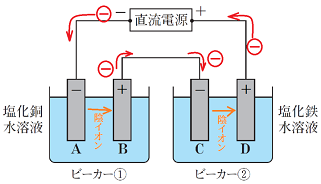
電源の-極から出た電子は、電極Aに向かうので、電極Aが陰極になり、ビーカー①の水溶液の陰イオンが電極Bに向かうので、電極Bが陽極になります。
電極Bが陰イオンから受け取った電子が電極Cに流れるので、電極Cが陰極に、同じように電極Dが陽極になります。
